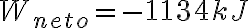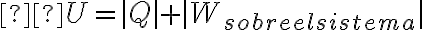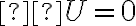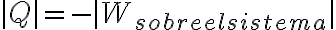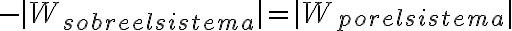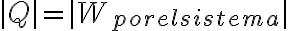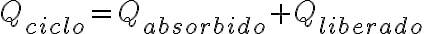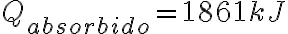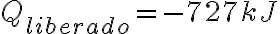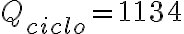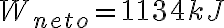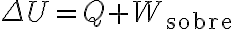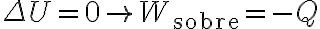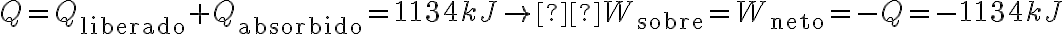Buenas tardes, tengo una duda con la resolución del ejercicio 3 del practico 8.En la parte C del dicho ejercicio, se nos pide el trabajo neto efectuado por el gas. En la solución se afirma que:
Sin embargo, si partimos de la primera ley de la termodinámica:
y considerando que para un ciclo
entonces tenemos:
Pero sabemos que:
Por lo tanto, podemos concluir que:
De las partes a y b, tenemos que:
donde:
Esto implica que:
Entonces el trabajo neto efectuado por el gas no tendría que ser:
No estoy seguro si estoy cometiendo un error conceptual o si la solución proporcionada está incorrecta.
Saludos!!