Buenas!
Mi duda es acerca de la parte d) del 9.8.
Me fije en las soluciones del parcial de 2017 y no comprendo por qué las temperaturas para obtener la menor variación de entropía posible son T1 y T3.
Buenas!
Mi duda es acerca de la parte d) del 9.8.
Me fije en las soluciones del parcial de 2017 y no comprendo por qué las temperaturas para obtener la menor variación de entropía posible son T1 y T3.
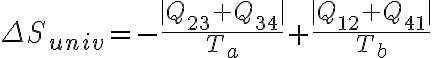 , podemos ver que el segundo término, positivo, disminuye al aumentar
, podemos ver que el segundo término, positivo, disminuye al aumentar 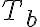 y el valor absoluto del primero, que tiene signo negativo, aumenta al disminuir
y el valor absoluto del primero, que tiene signo negativo, aumenta al disminuir 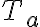 . Por lo tanto para disminuir
. Por lo tanto para disminuir 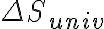 podemos disminuir
podemos disminuir 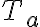 y aumentar
y aumentar 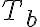 . Así que deberíamos ver cuál es la mínima
. Así que deberíamos ver cuál es la mínima 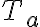 posible y la máxima
posible y la máxima 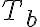 posible. Estas temperaturas de las reservas no pueden ser cualquier cosa. Por ejemplo, si analizamos el proceso isócoro 2-3, tenemos que el
posible. Estas temperaturas de las reservas no pueden ser cualquier cosa. Por ejemplo, si analizamos el proceso isócoro 2-3, tenemos que el 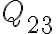 es entrante al sistema, por lo tanto para que se de este flujo de calor poniendo al gas en contacto con la reserva térmica a
es entrante al sistema, por lo tanto para que se de este flujo de calor poniendo al gas en contacto con la reserva térmica a 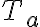 , necesitamos que la temperatura de la R.T sea siempre mayor a la del gas durante todo el proceso. Como la mayor temperatura que alcanza el gas durante este proceso es
, necesitamos que la temperatura de la R.T sea siempre mayor a la del gas durante todo el proceso. Como la mayor temperatura que alcanza el gas durante este proceso es 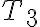 , tenemos que
, tenemos que 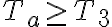 . Por lo que el valor más chico que puede tomar
. Por lo que el valor más chico que puede tomar 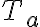 es
es 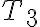 .
.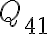 es saliente del sistema, entrante a la reserva. Para que el flujo de calor sea en este sentido, necesitamos que la temperatura de la reserva sea menor o igual a la del gas durante todo el proceso. La menor temperatura del gas durante este proceso es
es saliente del sistema, entrante a la reserva. Para que el flujo de calor sea en este sentido, necesitamos que la temperatura de la reserva sea menor o igual a la del gas durante todo el proceso. La menor temperatura del gas durante este proceso es 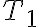 , por lo tanto
, por lo tanto 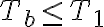 . Entonces el valor más grande que puede tomar
. Entonces el valor más grande que puede tomar 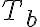 es
es 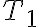 .
.