Hola.
La ecuación inicial es correcta. Podemos pensar de dónde sale para asegurarnos de que está bien. Si tomamos al gas como nuestro sistema, este sigue un proceso adiabático, por lo tanto Q=0 y, por la primera ley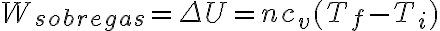 . Por otro lado, si estudiamos el sistema correspondiente a la masa
. Por otro lado, si estudiamos el sistema correspondiente a la masa 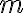 se tiene que el trabajo realizado sobre ella debe ser igual al cambio en su energía cinética:
se tiene que el trabajo realizado sobre ella debe ser igual al cambio en su energía cinética: 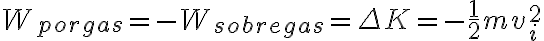 . De donde se puede despejar tu primera ecuación.
. De donde se puede despejar tu primera ecuación.
Después, como bien decís, se puede usar la relación para procesos adiabáticos cuasiestáticos: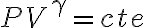 , aplicándola a los estados inicial y final del gas.
, aplicándola a los estados inicial y final del gas.
La ecuación de estado del gas ideal se puede aplicar en este caso, porque suponemos que el aire se comporta como un gas ideal, como dice la letra.
Así que el razonamiento es correcto, revisá las cuentas que puede haber un error ahí.
Saludos.
La ecuación inicial es correcta. Podemos pensar de dónde sale para asegurarnos de que está bien. Si tomamos al gas como nuestro sistema, este sigue un proceso adiabático, por lo tanto Q=0 y, por la primera ley
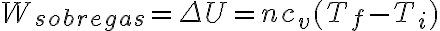 . Por otro lado, si estudiamos el sistema correspondiente a la masa
. Por otro lado, si estudiamos el sistema correspondiente a la masa 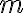 se tiene que el trabajo realizado sobre ella debe ser igual al cambio en su energía cinética:
se tiene que el trabajo realizado sobre ella debe ser igual al cambio en su energía cinética: 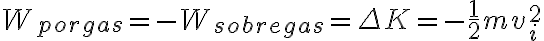 . De donde se puede despejar tu primera ecuación.
. De donde se puede despejar tu primera ecuación.Después, como bien decís, se puede usar la relación para procesos adiabáticos cuasiestáticos:
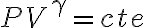 , aplicándola a los estados inicial y final del gas.
, aplicándola a los estados inicial y final del gas.La ecuación de estado del gas ideal se puede aplicar en este caso, porque suponemos que el aire se comporta como un gas ideal, como dice la letra.
Así que el razonamiento es correcto, revisá las cuentas que puede haber un error ahí.
Saludos.
